Le moment « eurêka »
Quand on fait des travaux de recherche véritablement novateurs, vient souvent un moment de clarté – un moment où il nous apparaît nettement qu’une découverte a le potentiel de révolutionner la science et la médecine telles que nous les connaissons. C’est à la suite d’un tel moment « eurêka » qu’Alnylam a été fondée.
Écoutez Phil Sharp et Craig Mello, Ph. D., cofondateurs de notre entreprise, parler de la découverte des ARNi et de la naissance d’Alnylam.
La vidéo suivante est en anglais
Mode d’action des ARNi thérapeutiques
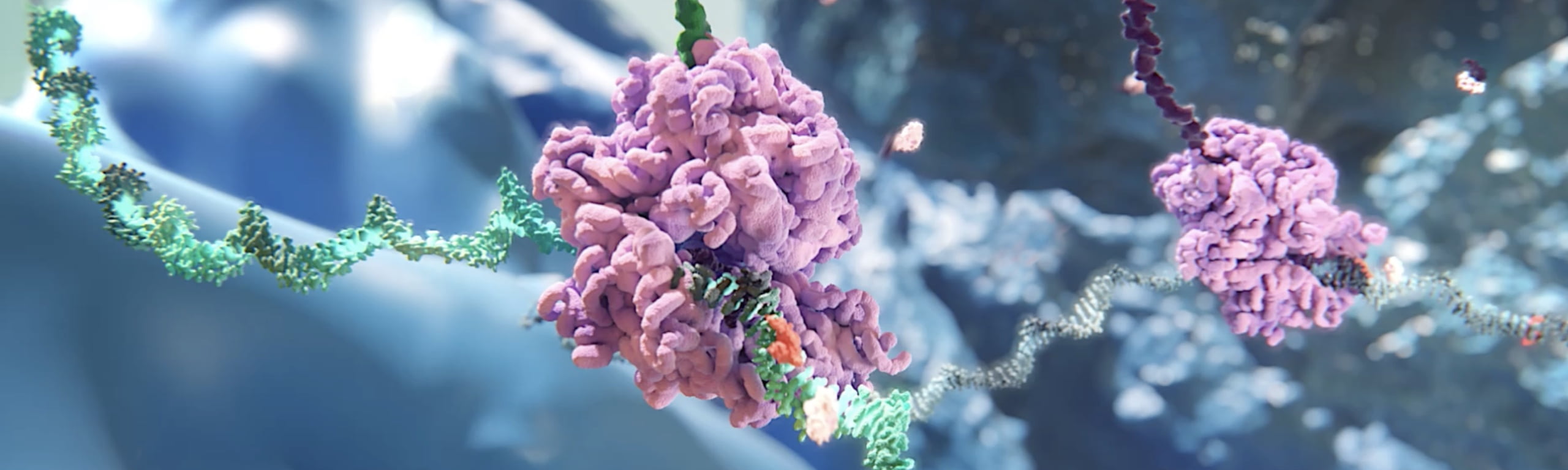
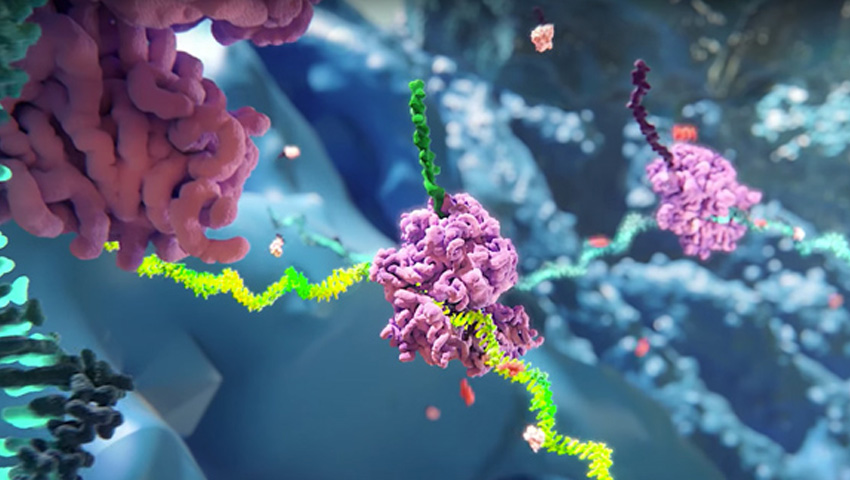
L’interférence par ARN est un processus de régulation négative des gènes qui survient naturellement dans les cellules et qui se trouve à l’une des frontières les plus prometteuses et où les progrès sont les plus rapides dans les domaines de la biologie et de la mise au point de médicaments.
Les ARNi thérapeutiques constituent une nouvelle classe de médicaments exploitant le mécanisme biologique naturel de l’interférence par ARN. De petits ARN interférents (pARNi), les molécules qui interviennent dans l’interférence par ARN et qui constituent la plateforme thérapeutique d’Alnylam, agissent « en amont » des médicaments actuels grâce à leur puissante action de régulation négative de l’ARN messager (ARNm), le précurseur génétique qui code les protéines causant la maladie, et préviennent ainsi la formation de ces protéines. Il s’agit d’une approche révolutionnaire qui pourrait transformer la prise en charge des patients atteints de maladies génétiques et d’autres affections.
Nos ARNi thérapeutiques font appel à deux mécanismes distincts pour assurer le transport des pARNi jusqu’aux cellules cibles : des nanoparticules lipidiques (NPL) et la conjugaison avec des molécules de N-acétylgalactosamine.
Voyez comment les ARNi thérapeutiques agissent dans les cellules. La vidéo suivante est en anglais
5 caractéristiques clés d’une approche reposant sur les ARNi thérapeutiques
Les ARNi sont généralement considérés comme se trouvant à l’une des frontières les plus prometteuses et où les progrès sont les plus rapides dans les domaines de la biologie et de la mise au point de médicaments.
1. La capacité à profiter d’un mécanisme naturel. L’interférence par ARN est un mécanisme de régulation de l’expression des gènes qui survient naturellement dans toutes les cellules mammaliennes, et qui se fait par l’entremise de molécules qu’on appelle petits ARN interférents (pARNi). En exploitant ce mécanisme biologique naturel, les ARNi thérapeutiques peuvent facilement être conçus pour être très sélectifs.
2. Le pouvoir catalytique. Le complexe enzymatique RISC (de l’anglais RNA-Induced Silencing Complex), qui intervient dans le processus d’interférence par ARN pour inactiver l’ARNm, ne requiert qu’un seul pARNi pour cliver un grand nombre d’ARNm cibles. Autrement dit, les pARNi agissent de manière catalytique.
3. La capacité de cibler pratiquement n’importe quelle protéine. Contrairement aux petites molécules et aux anticorps (qui constituent la plupart des médicaments d’aujourd’hui), il est possible de concevoir des pARNi ciblant la transcription des ARNm de n’importe quel gène.
Cette caractéristique permet de croire qu’il est possible de mettre au point des ARNi thérapeutiques ciblant des protéines habituellement considérées comme n’étant pas des « cibles thérapeutiques ». En outre, certaines maladies peuvent être causées par une mutation dans un seul exemplaire des gènes (c.-à-d. dans un seul allèle); dans ce cas, un pARNi particulier peut cibler la mutation qui provoque la maladie en laissant l’allèle normal intact. Nous pensons qu’il est possible de concevoir des ARNi thérapeutiques ciblant n’importe quel gène qui intervient dans la cause ou le processus de la maladie.
4. L’action « en amont » des médicaments actuels. Les ARNi thérapeutiques que nous mettons au point peuvent bloquer la production des protéines causant les maladies.
Grâce à l’interférence par ARN, nous croyons qu’il est possible d’arriver à museler de manière constante et réglable la production des protéines responsables des maladies, quels que soient les taux de ces protéines dans le sang, afin de maîtriser et de prendre en charge la maladie. Pour faire une analogie, disons que l’emploi des ARNi thérapeutiques équivaut à stopper un dégât d’eau en fermant le robinet, alors qu’avec les autres médicaments, on ne fait qu’éponger l’eau.
5. La simplification de la découverte de bons candidats thérapeutiques. Nous croyons que l’interférence par ARN est un moyen plus direct d’identifier les bons candidats thérapeutiques, ce qui peut se faire au moyen d’outils bioinformatiques permettant de sélectionner des séquences qui complètent l’ARNm cible. Les étapes suivantes du processus de sélection d’un ARNi bon candidat thérapeutique sont la synthèse et la mise à l’essai des pARNi. En outre, les pARNi les plus prometteurs peuvent être conçus pour agir chez un grand éventail d’espèces, ce qui pourrait simplifier l’extrapolation à l’humain des données relatives aux modèles animaux. Certaines modifications chimiques pourraient aussi être apportées aux pARNi pour leur conférer des propriétés les rendant semblables à des médicaments, par exemple pour les stabiliser lorsqu’ils sont administrés dans la circulation. Enfin, différents moyens d’administration des ARNi thérapeutiques expérimentaux ont été mis au point afin d’assurer de manière constante et ciblée la régulation de l’expression des gènes dans des organes particuliers, par exemple le foie.
Nous avons en outre observé une corrélation très étroite entre la régulation négative ciblée obtenue chez les modèles animaux et celle qui a été obtenue au cours des essais cliniques chez l’humain, ce qui nous aidera probablement à poursuivre au stade des essais cliniques la recherche sur les ARNi thérapeutiques commencée au stade préclinique. Pour toutes ces raisons, nous croyons que nos ARNi thérapeutiques expérimentaux constituent une approche hautement modulaire et reproductible pour la découverte et la mise au point de médicaments.